IA et diagnostic médical : une révolution en marche
Comment l’IA transforme le diagnostic en radiologie, dermatologie et pathologie.
La découverte de nouveaux médicaments est un processus long, coûteux et risqué : 10 à 15 ans de recherche, plus d’un milliard d’euros d’investissement, et 90 % d’échec en essais cliniques. L’intelligence artificielle change la donne. De la prédiction des structures protéiques avec AlphaFold à l’optimisation des essais cliniques, cet article explore comment l’IA accélère et transforme la recherche pharmaceutique.
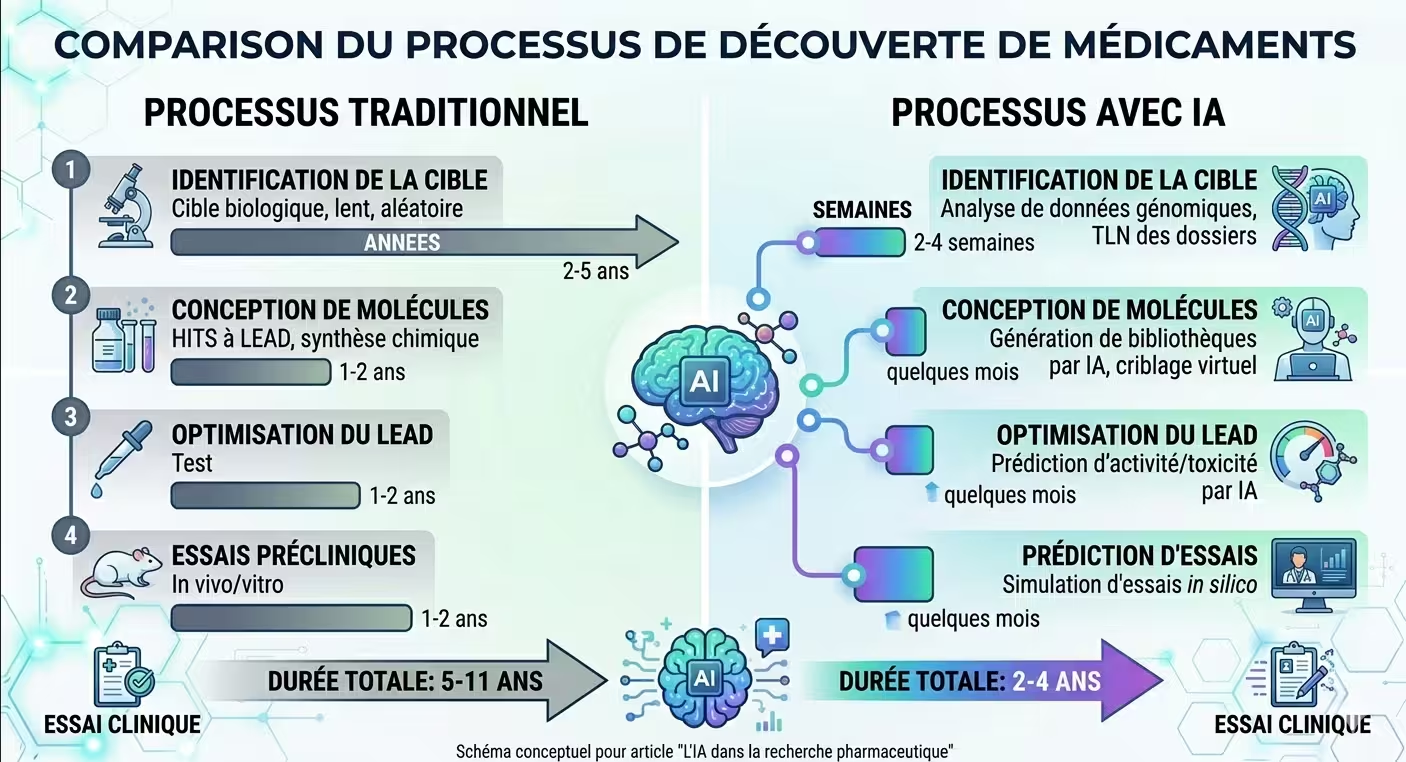
Figure 1 : L'IA accélère chaque étape de la découverte de médicaments, de la cible biologique à l'essai clinique.
La recherche pharmaceutique traditionnelle suit un parcours long et incertain : de la découverte d’une cible biologique (protéine impliquée dans une maladie) à la mise sur le marché d’un médicament, il faut en moyenne 10 à 15 ans et un investissement estimé entre 1 et 2 milliards d’euros. Le taux d’échec est colossal : plus de 90 % des candidats-médicaments échouent en essais cliniques, souvent lors des phases avancées.
Selon le rapport « Clinical Development Success Rates » (2025), la probabilité qu’un médicament entrant en phase 1 aboutisse à une autorisation de mise sur le marché est d’environ 7 % en oncologie, et de 12 % toutes pathologies confondues.
L’intelligence artificielle intervient à chaque étape de ce processus pour réduire les coûts, accélérer les délais et augmenter les chances de succès. Elle promet de passer d’une approche par essais-erreurs à une approche prédictive et personnalisée.
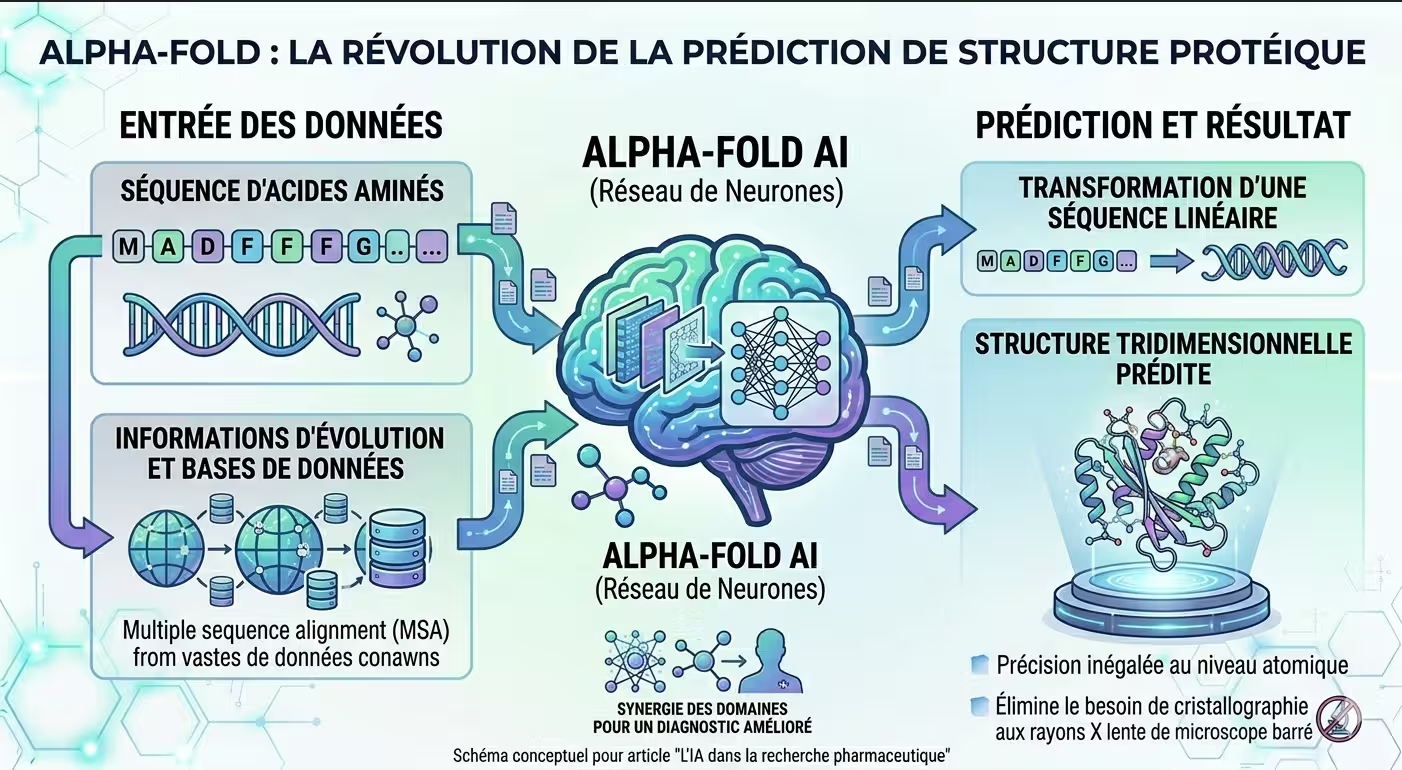
Figure 2 : AlphaFold prédit la structure tridimensionnelle des protéines avec une précision inégalée, accélérant la découverte de cibles thérapeutiques.
En 2020, DeepMind (filiale d’Alphabet) a présenté AlphaFold 2, un système d’IA capable de prédire la structure tridimensionnelle des protéines avec une précision inégalée. En 2024, AlphaFold 3 a étendu ses capacités aux interactions protéine-ligand, protéine-ADN, et aux biomolécules complexes.
La structure d’une protéine détermine sa fonction et ses interactions avec d’autres molécules. Connaître cette structure est essentiel pour concevoir des médicaments capables de se fixer sur la protéine cible. Avant AlphaFold, déterminer une structure protéique expérimentalement (par cristallographie ou cryo-microscopie électronique) prenait des mois, voire des années, et n’était possible que pour une fraction des protéines connues.
AlphaFold a prédit les structures de plus de 200 millions de protéines (pratiquement toutes les protéines connues) et les a rendues accessibles via la base de données AlphaFold Protein Structure Database. Cette avancée est considérée par de nombreux experts comme l’une des plus importantes de l’histoire de la biologie structurale.
Des milliers d’équipes de recherche utilisent quotidiennement AlphaFold pour accélérer la phase de découverte. Selon une enquête de Nature (2025), plus de 60 % des laboratoires pharmaceutiques ont intégré AlphaFold dans leur pipeline de découverte de cibles.
AlphaFold prédit les structures statiques des protéines, mais pas leurs changements conformationnels (mouvements) ni leurs interactions complexes dans l’environnement cellulaire réel. Des travaux sont en cours pour développer des modèles capables de simuler la dynamique protéique.
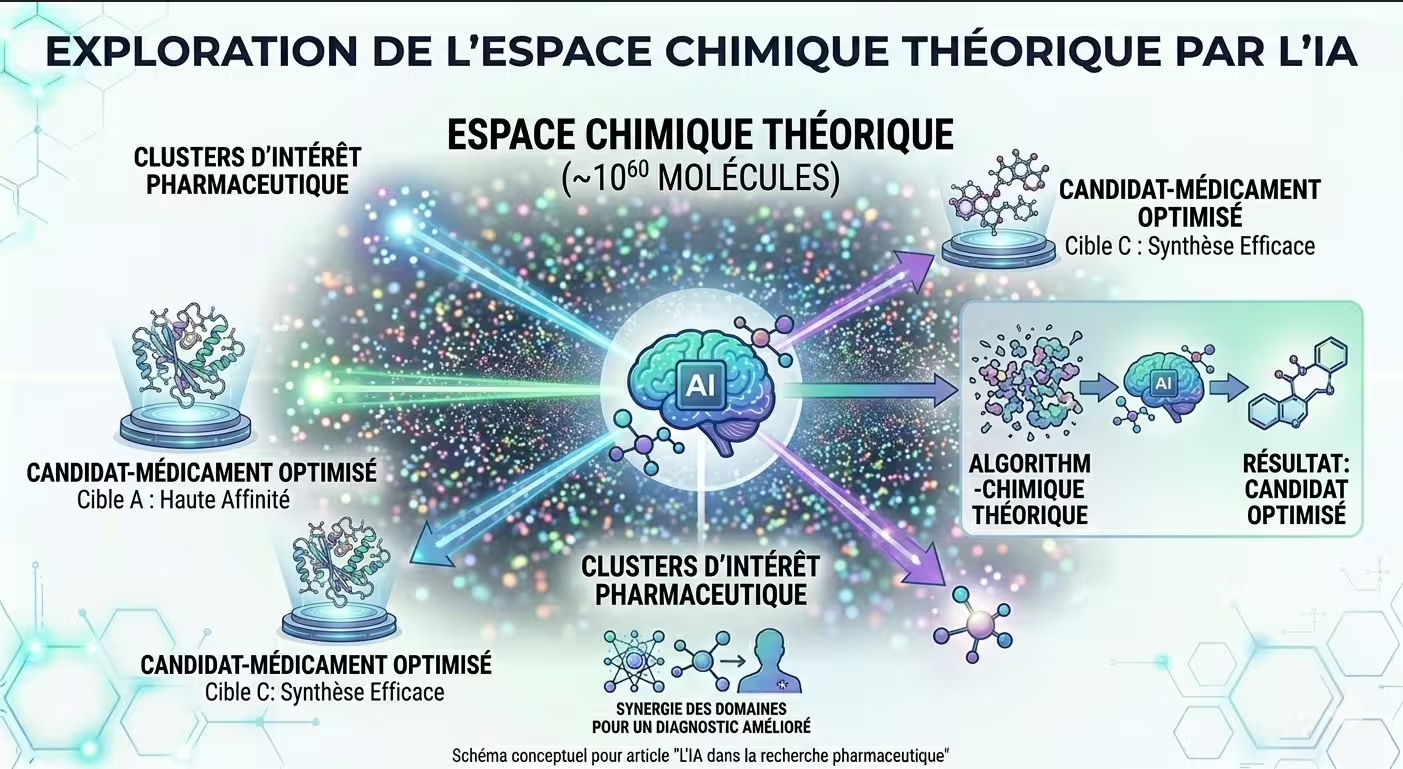
Figure 3 : L'IA explore un espace chimique théorique de 10⁶⁰ molécules pour générer des candidats-médicaments optimisés.
Une fois la cible biologique identifiée (par exemple, une protéine impliquée dans le cancer), l’IA peut générer des molécules candidates susceptibles de s’y fixer. Des modèles génératifs (réseaux antagonistes génératifs, autoencodeurs variationnels, modèles de diffusion) explorent un espace chimique théorique de 10⁶⁰ molécules possibles – bien au-delà des capacités humaines ou des criblages robotisés traditionnels.
L’une des principales causes d’échec en développement précoce est l’absorption, distribution, métabolisme, excrétion et toxicité (ADME-Tox) défavorables. L’IA permet aujourd’hui de prédire ces propriétés avant toute synthèse en laboratoire, éliminant des milliers de candidats non viables.
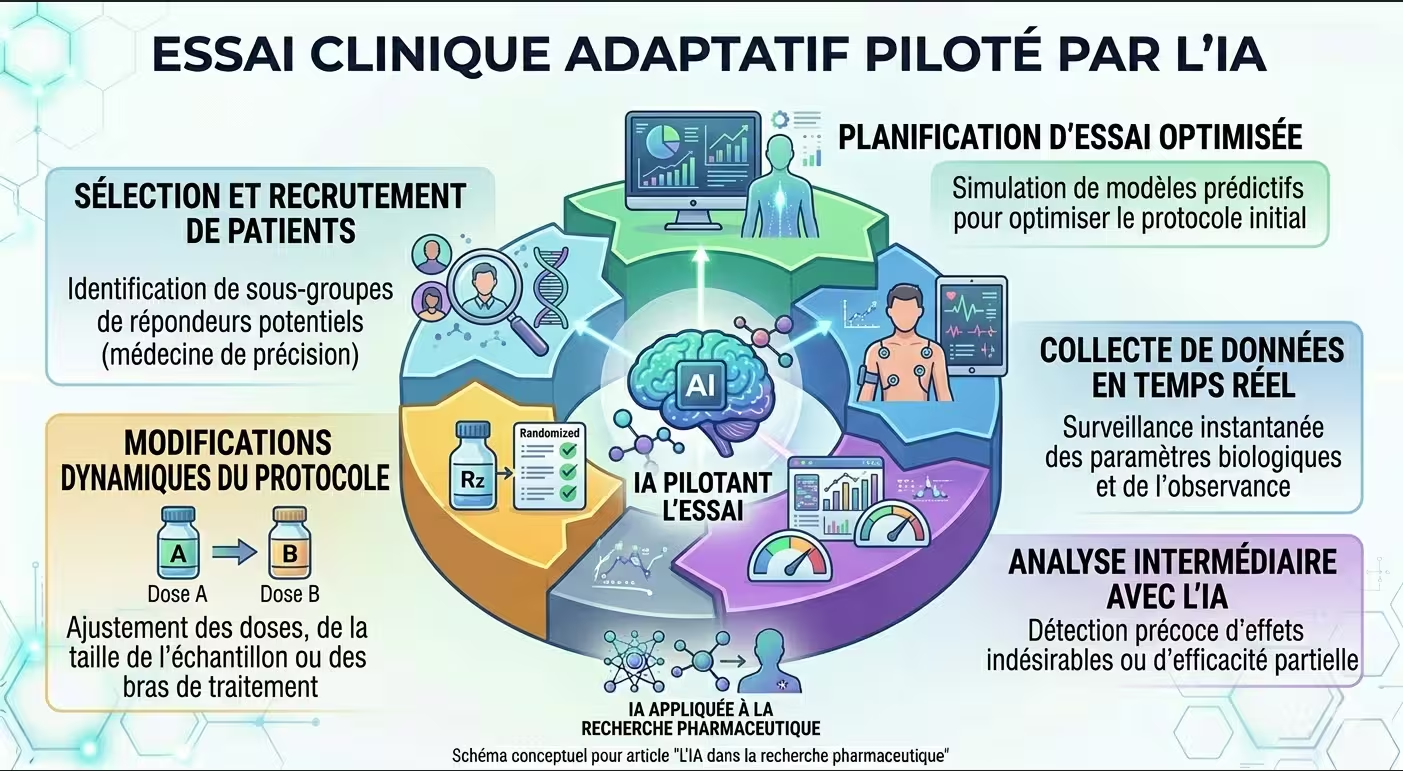
Figure 4 : Les essais cliniques adaptatifs utilisent l'IA pour ajuster le protocole en temps réel, réduisant la durée et les coûts.
Les essais cliniques représentent jusqu’à 70 % du coût de développement d’un médicament. L’IA intervient à plusieurs niveaux pour les optimiser :
Le recrutement est l’un des goulots d’étranglement majeurs : plus de 80 % des essais connaissent des retards de recrutement. L’IA analyse les dossiers médicaux électroniques (en respectant la confidentialité) pour identifier les patients éligibles, réduisant les délais de plusieurs mois. Des startups comme Deep 6 AI ou Antidote proposent ces solutions.
Les essais adaptatifs utilisent l’IA pour ajuster le protocole en cours de route : modification des doses, arrêt précoce des bras inefficaces, ou redirection des ressources vers les groupes les plus prometteurs. Cette approche peut réduire le nombre de patients nécessaires et la durée totale de l’essai.
En 2025, le premier essai clinique entièrement piloté par l’IA a été lancé dans le cadre du partenariat entre Insilico Medicine et Sanofi. L’IA a conçu la molécule, optimisé le protocole, et géré le recrutement.
| Médicament / Candidat | Développeur | Rôle de l’IA | Statut (2026) |
|---|---|---|---|
| INS018_055 (fibrose pulmonaire idiopathique) | Insilico Medicine | IA a découvert la cible, généré la molécule, et optimisé le protocole. Première molécule IA en phase 2 clinique (2024). | Phase 2 en cours, résultats intermédiaires prometteurs. |
| DSP-1181 (troubles obsessionnels compulsifs) | Sumitomo Pharma / Exscientia | IA a généré la molécule en 12 mois (contre 4-5 ans en traditionnel). | Phase 1 terminée, développement poursuivi. |
| REC-994 (caverne malformation) | Recursion Pharmaceuticals | Plateforme IA de criblage à haut contenu, analyse d’images cellulaires. | Phase 2 en cours. |
| Baricitinib (COVID-19) | Eli Lilly / BenevolentAI | IA a identifié ce médicament existant comme candidat potentiel pour le COVID-19 en février 2020. | Autorisation d’urgence obtenue, utilisé dans plusieurs pays. |
Ces exemples illustrent l’accélération : là où un développement traditionnel prend 4 à 5 ans pour arriver à un candidat clinique, l’IA peut le faire en 12 à 18 mois.
Les prédictions de l’IA restent des prédictions. Un candidat généré in silico doit encore être synthétisé, testé in vitro, puis in vivo, avant de pouvoir entrer en clinique. Le taux de validation expérimentale reste un défi. Certaines molécules prédites comme « parfaites » en simulation se révèlent inefficaces ou toxiques en laboratoire.
Les agences réglementaires (FDA, EMA) évoluent. La FDA a publié en 2025 un cadre pour l’utilisation de l’IA dans le développement de médicaments, mais exige encore des preuves expérimentales robustes. L’opacité algorithmique (les « boîtes noires ») est un point de friction : les régulateurs demandent des modèles interprétables ou une documentation exhaustive des données d’entraînement.
L’IA a besoin de données massives et de qualité. Or, les données pharmaceutiques sont souvent fragmentées, hétérogènes, ou propriétaires. Les initiatives comme le Cancer Research UK’s National Cancer Imaging Repository ou le European Health Data Space visent à structurer et partager ces données, mais le chemin est long.
L’intégration de l’IA dans les processus de recherche pharmaceutique nécessite des investissements significatifs et un changement culturel. Les grandes sociétés pharmaceutiques (Novartis, Pfizer, Roche) ont massivement investi, mais la transformation est progressive.
Tous les géants pharmaceutiques ont désormais des divisions IA :
De nombreuses startups sont nées avec l’IA comme cœur de leur R&D :
Les géants technologiques investissent également :
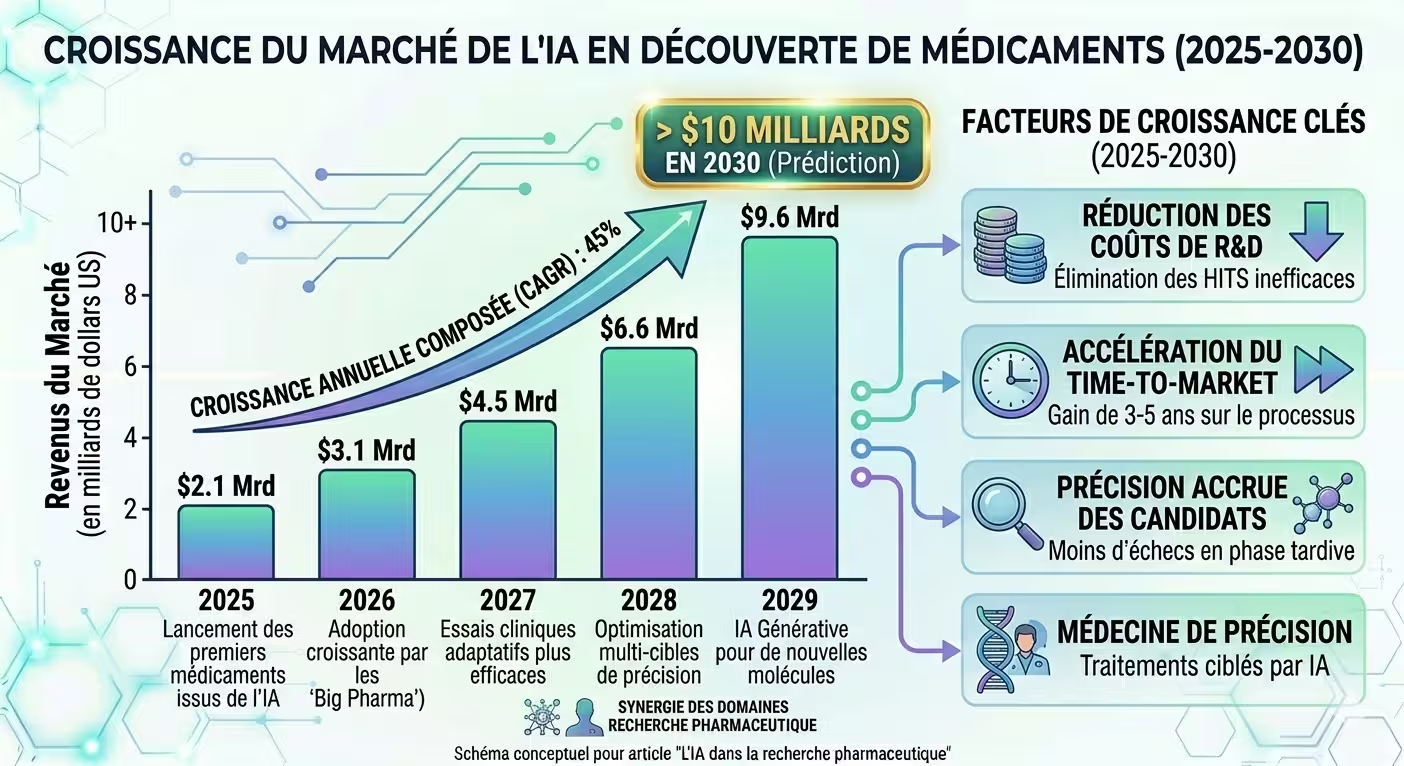
Figure 5 : Le marché de l'IA en découverte de médicaments devrait atteindre plus de 10 milliards de dollars en 2030, avec une croissance annuelle de 45%.
L’émergence de modèles fondation (large language models appliqués à la biologie) promet de transformer le domaine. Des modèles comme Evo (Arc Institute) ou AlphaProteo (DeepMind) peuvent générer directement des protéines fonctionnelles sur mesure. Ces modèles, entraînés sur des milliards de séquences génomiques, pourraient permettre de concevoir des médicaments « à la demande » pour des cibles spécifiques.
Les essais cliniques décentralisés (DCT) combinant capteurs connectés, IA et télémédecine devraient se généraliser. Objectif : réduire les coûts de 30 % et les délais de 20 % d’ici 2030.
L’IA permettra de développer des traitements pour des populations très restreintes, voire pour un patient unique. Des cas de « n-of-1 trials » (essais cliniques à un seul patient) utilisant l’IA sont déjà documentés pour des maladies génétiques rares.
Selon Grand View Research (2026), le marché de l’IA en découverte de médicaments devrait passer de 1,5 milliard de dollars en 2025 à plus de 10 milliards en 2030, avec un taux de croissance annuel de 45 %.
AlphaFold est un système d’IA développé par DeepMind qui prédit la structure tridimensionnelle des protéines avec une précision comparable aux méthodes expérimentales. Connaître la structure des protéines est essentiel pour concevoir des médicaments capables de les cibler. AlphaFold a prédit les structures de plus de 200 millions de protéines, accélérant considérablement la phase de découverte.
La phase de découverte (identification de la cible, génération d’une molécule candidate) peut être réduite de 4-5 ans à 12-18 mois avec l’IA. Cependant, les phases de développement préclinique et clinique (essais sur humains) restent longues (5 à 8 ans). L’objectif est de réduire les échecs tardifs grâce à une meilleure prédiction précoce.
À ce jour (2026), aucun médicament développé entièrement par IA n’a encore obtenu d’autorisation de mise sur le marché. Plusieurs candidats sont en phase 2 et phase 3 clinique. Les experts estiment que le premier médicament « IA » pourrait arriver d’ici 2027-2028.
Non. L’IA est un outil d’assistance puissant, mais elle ne remplace pas l’expertise des chimistes, biologistes et cliniciens. Elle automatise certaines tâches (criblage, prédiction), permet d’explorer plus d’hypothèses, mais la validation expérimentale et la décision humaine restent centrales.
La FDA a publié en 2025 un cadre pour l’utilisation de l’IA dans le développement de médicaments, avec un accent sur la transparence algorithmique et la validation. L’EMA (Europe) suit une approche similaire. Les deux agences exigent encore des preuves expérimentales robustes en complément des prédictions.
Les défis incluent : la fiabilité des prédictions (validation expérimentale nécessaire), l’opacité des modèles (besoin d’explicabilité), la qualité et la disponibilité des données, l’intégration dans les processus existants, et l’acceptation par les régulateurs.
L’intelligence artificielle ne remplacera pas les chercheurs en pharmacie, mais elle transforme en profondeur leurs méthodes et leurs outils. De la prédiction des structures protéiques avec AlphaFold à la génération de nouvelles molécules, en passant par l’optimisation des essais cliniques, l’IA promet de réduire les coûts, d’accélérer les délais et d’augmenter les taux de succès d’un processus historiquement long et risqué.
Les premiers candidats-médicaments issus de l’IA sont désormais en phase clinique avancée. Leurs résultats, attendus dans les prochaines années, détermineront si la promesse se concrétise. Une chose est sûre : la recherche pharmaceutique ne sera plus jamais la même. L’IA est devenue un compagnon indispensable dans la quête de nouveaux traitements pour les maladies les plus dévastatrices.