1. Qu’est-ce que le génome humain et pourquoi le cartographier ?
Le génome humain, c’est l’intégralité de l’information génétique contenue dans chacune de nos cellules (à l’exception des globules rouges). Cette information est écrite dans une molécule appelée ADN (acide désoxyribonucléique), qui se présente sous la forme d’une double hélice. L’ADN est composé de quatre « lettres » chimiques — l’adénine (A), la thymine (T), la guanine (G) et la cytosine (C) — qui s’agencent en séquences de trois milliards de paires de bases. Ces séquences forment environ 20 000 à 25 000 gènes, eux-mêmes organisés en 23 paires de chromosomes.
Cartographier le génome humain, c’est établir la séquence exacte de ces trois milliards de lettres, et identifier l’emplacement et la fonction des gènes. C’est une entreprise titanesque, comparable à la découverte de la structure du système solaire ou à la classification du vivant par Linné. L’enjeu est immense : comprendre les mécanismes de la vie, mais surtout identifier les variations génétiques responsables de maladies (cancer, maladies rares, diabète, Alzheimer, etc.) et développer des traitements ciblés, voire des thérapies géniques correctrices.
Chiffre clé
Seulement 1 à 2 % du génome humain code pour des protéines (les gènes « classiques »). Le reste — longtemps appelé « ADN poubelle » — contient des éléments régulateurs, des séquences non codantes, et des vestiges évolutifs. L’IA aide aujourd’hui à décrypter ces régions longtemps ignorées, qui jouent un rôle crucial dans de nombreuses maladies.

Infographie n°1 – Le génome humain en chiffres : 3 milliards de paires de bases, 20 000-25 000 gènes, 23 paires de chromosomes. Image conservée de l’article original.
2. Historique : de la découverte de l’ADN à la cartographie complète
L’aventure de la génomique moderne commence en 1953, lorsque James Watson et Francis Crick découvrent la structure en double hélice de l’ADN, une découverte qui leur vaudra le prix Nobel. Pendant les décennies suivantes, les progrès sont lents : on apprend à décrypter de courts fragments d’ADN (séquençage Sanger, 1977), mais l’idée de séquencer l’intégralité du génome humain semble alors relever de la science-fiction.
En 1990, le projet international Human Genome Project (HGP) est officiellement lancé, coordonnant 20 institutions dans six pays (États-Unis, Royaume-Uni, France, Allemagne, Japon, Chine). L’objectif : obtenir la séquence complète du génome humain d’ici 2005. C’est une course de vitesse : en parallèle, la société privée Celera Genomics, dirigée par Craig Venter, se lance dans la même aventure avec des méthodes concurrentes. La compétition aboutit à une publication conjointe en 2001 (première ébauche), puis à l’achèvement officiel du projet en 2003, avec deux ans d’avance. Coût total : environ 3 milliards de dollars.
1953
découverte de la structure de l’ADN
Watson & Crick
1990-2003
Human Genome Project
3 G$ / 13 ans
2026
séquençage complet ≈ 600 € / 1 jour
NGS
Depuis 2003, les technologies de séquençage n’ont cessé de progresser. Le séquençage de nouvelle génération (NGS) a remplacé les méthodes artisanales par des procédés industriels, automatisés et parallélisés. En 2026, le coût d’un génome complet est tombé à environ 600 euros (contre 10 000 € en 2015), et le délai d’obtention à moins de 24 heures. Cette baisse spectaculaire a ouvert la voie à des applications médicales à grande échelle.
3. Le séquençage du génome humain : une avancée vers la médecine de précision
Le séquençage du génome consiste à déterminer l’ordre exact des paires de bases (les lettres A, T, G, C) dans un segment d’ADN. Les premiers procédés, comme le séquençage de Sanger (prix Nobel 1980), étaient extrêmement laborieux : il fallait plusieurs années et des centaines de millions de dollars pour séquencer un génome. Les technologies de nouvelle génération (NGS) ont radicalement changé la donne.

Infographie n°2 – Les étapes du séquençage de nouvelle génération (NGS), image conservée de l’article original.
Des coûts en chute libre
La loi de Moore (qui veut que la puissance des ordinateurs double tous les deux ans) a trouvé son équivalent en génomique : la « loi de Carlson », selon laquelle le coût du séquençage est divisé par deux tous les 18 mois, soit une baisse encore plus rapide que celle des transistors. En 2026, un génome complet séquencé en routine clinique coûte environ 600 euros, un prix qui devient abordable pour un nombre croissant de patients. À titre de comparaison, en 2001, le coût était de 100 millions de dollars.
Des applications médicales concrètes
Grâce à cette accessibilité, le séquençage génomique est désormais utilisé en routine pour : identifier des mutations génétiques responsables de maladies rares (diagnostic étiologique), guider les traitements anticancéreux (onco-génétique), prédire la réponse à certains médicaments (pharmacogénomique), ou encore dépister des prédispositions génétiques à des maladies tardives (maladie de Huntington, certains cancers héréditaires). Des programmes nationaux comme « France Médecine Génomique 2025 » (devenu 2030) ont permis de séquencer des centaines de milliers de patients.
4. L’IA : un accélérateur pour l’analyse et l’interprétation du génome
Si les technologies de séquençage rendent la lecture de l’ADN plus accessible, l’analyse de l’immense quantité de données générées nécessite des outils encore plus puissants. C’est là que l’intelligence artificielle intervient, comme un traducteur universel entre le langage de la nature (l’ADN) et le langage des médecins.
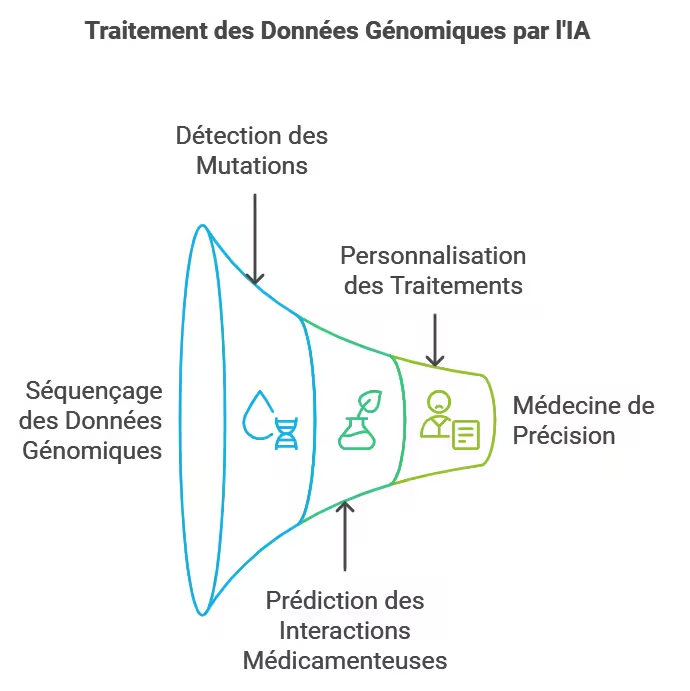
Infographie n°3 – L’IA au cœur de l’analyse génomique, image conservée de l’article original.
Détection de mutations pathogènes
Les algorithmes de machine learning, et plus récemment les modèles de deep learning (réseaux de neurones profonds), sont capables d’analyser des millions de variants génétiques en quelques heures. Ils distinguent les variations bénignes (polymorphismes naturels) des mutations véritablement pathogènes, en s’appuyant sur des bases de données de référence (ClinVar, gnomAD) et sur des modèles prédictifs de l’impact des variants sur la fonction des protéines. Des outils comme VarSome, Franklin ou Emedgene sont désormais utilisés en routine dans les laboratoires de génétique médicale.
Prédiction des interactions médicamenteuses (pharmacogénomique)
Notre ADN influence la manière dont nous métabolisons les médicaments. Certaines personnes sont des « métaboliseurs lents » (risque de surdosage), d’autres des « métaboliseurs rapides » (risque de sous-dosage). L’IA analyse les variants génétiques des enzymes du métabolisme (cytochromes P450, etc.) pour prédire la réponse individuelle à des centaines de médicaments. Des plateformes comme YouScript ou Geneyx intègrent ces prédictions dans les dossiers médicaux électroniques, aidant les médecins à prescrire la bonne dose dès la première prescription (évitant les tâtonnements).
Personnalisation des traitements (médecine de précision)
En croisant les données génomiques avec les données cliniques (imagerie, antécédents, mode de vie), l’IA peut proposer un traitement « sur mesure » pour un patient donné. C’est particulièrement avancé en cancérologie : le profil génomique d’une tumeur (ses mutations) oriente vers une thérapie ciblée (un médicament qui bloque spécifiquement la protéine mutée) plutôt qu’une chimiothérapie « standard » aux effets secondaires lourds.
5. Applications concrètes : cancer, maladies rares, pharmacogénomique
Cancer : la théranostique à l’ère de l’IA
Chaque tumeur a son propre « paysage génétique », avec des mutations qui la rendent unique. Des plateformes comme Foundation Medicine (États-Unis) ou Sophia Genetics (Europe) utilisent l’IA pour analyser le génome des tumeurs et identifier des biomarqueurs prédictifs. Par exemple, la présence d’une mutation du gène EGFR dans un cancer du poumon oriente vers un traitement par inhibiteurs de tyrosine kinase (Gefitinib, Osimertinib) bien plus efficace que la chimiothérapie standard. L’IA permet aussi de détecter des mutations rares qui seraient passées inaperçues lors d’une analyse manuelle.
Maladies génétiques rares : mettre fin à l’errance diagnostique
On estime à 300 millions le nombre de personnes dans le monde atteintes d’une maladie rare, dont 80 % ont une origine génétique. Le diagnostic prend en moyenne 5 à 7 ans (parcours du combattant médical). Des entreprises comme Rare Genomics, FDNA (qui analyse les traits du visage pour suggérer des syndromes génétiques) ou Genomenon utilisent l’IA pour accélérer ce diagnostic. En croisant les données génomiques du patient avec les bases de données de la littérature médicale, l’IA peut identifier la mutation responsable en quelques jours, là où une équipe humaine mettrait des mois.
Pharmacogénomique : la prescription de précision
En 2026, de plus en plus d’hôpitaux intègrent un test pharmacogénomique avant la prescription de médicaments à marge thérapeutique étroite (anticoagulants comme la warfarine, antidépresseurs, antiépileptiques, certaines chimiothérapies). L’IA analyse les variants génétiques du patient et propose un dosage initial optimal, réduisant les risques d’effets secondaires graves et d’hospitalisations évitables. Le modèle économique commence à être validé : des études montrent que le coût du test (environ 200-300 €) est largement compensé par les économies liées aux complications évitées.
6. AlphaFold et la révolution de la prédiction des structures protéiques
Une mention spéciale mérite AlphaFold, le système d’intelligence artificielle développé par DeepMind (Google). Pour comprendre le lien avec le génome : l’ADN code pour des protéines (via le dogme central de la biologie moléculaire : ADN → ARN → protéine). La fonction d’une protéine dépend de sa forme tridimensionnelle (sa structure). Prédire cette structure à partir de la seule séquence d’acides aminés était un défi vieux de 50 ans, le « problème de la prédiction de la structure des protéines ».
En 2020, AlphaFold a résolu ce problème avec une précision comparable aux méthodes expérimentales (cristallographie aux rayons X, cryo-microscopie électronique). En 2024, DeepMind a publié la structure de plus de 200 millions de protéines — pratiquement toutes les protéines connues. Cette base de données, librement accessible (AlphaFold Protein Structure Database), est une mine d’or pour la recherche médicale. Elle permet de comprendre comment une mutation génétique altère la structure d’une protéine, donc sa fonction, et potentiellement de concevoir des médicaments qui se lient spécifiquement à la forme mutée.
AlphaFold 3 (2024-2025)
La version AlphaFold 3, annoncée en 2024, va encore plus loin : elle prédit non seulement les structures des protéines seules, mais aussi leurs interactions avec d’autres molécules (ADN, ARN, ligands, ions). Cela ouvre la voie à une modélisation complète des voies métaboliques et à la conception de médicaments assistée par IA, accélérant considérablement la recherche pharmaceutique.
7. Biobanques et données massives : le carburant de l’IA génomique
Les algorithmes d’IA ont besoin de grandes quantités de données pour apprendre. En génomique, ces données proviennent des biobanques : des collections d’échantillons biologiques (sang, tissus) et de données associées (séquençage, dossiers médicaux, imagerie, questionnaires).
UK Biobank : la référence mondiale
La UK Biobank a recueilli les données génomiques, médicales et de mode de vie de 500 000 Britanniques. Ces données, anonymisées, sont mises à disposition des chercheurs du monde entier. L’IA a permis de nombreuses découvertes : identification de nouveaux gènes de prédisposition au diabète, corrélation entre variants génétiques et réponse à l’exercice physique, prédiction du risque de maladies cardiovasculaires.
France : le projet France Génomique
La France s’est dotée d’une infrastructure nationale (France Génomique, puis France Médecine Génomique 2025/2030) avec l’objectif de séquencer 500 000 génomes d’ici 2030, principalement dans le cadre de soins (cancer, maladies rares). Les données sont centralisées dans l’Institut de génomique (CEA) et accessibles aux chercheurs sous conditions. L’IA est utilisée pour l’analyse à grande échelle, avec des plateformes comme Outy (plateforme nationale d’analyse génomique).
All of Us (NIH, États-Unis)
Le programme américain « All of Us » vise à séquencer 1 million de personnes, avec un effort particulier pour inclure des populations historiquement sous-représentées (minorités ethniques). L’objectif est de construire une base de données diverse pour éviter les biais algorithmiques.
500 000
génomes séquencés (UK Biobank)
référence mondiale
500 000
objectif France 2030
France Génomique
1 million
objectif « All of Us » (USA)
NIH
8. Enjeux éthiques et défis à surmonter : confidentialité, biais, accès
La génomique et l’IA ouvrent des perspectives révolutionnaires, mais elles soulèvent également des défis éthiques et technologiques majeurs, qu’il est essentiel d’aborder.
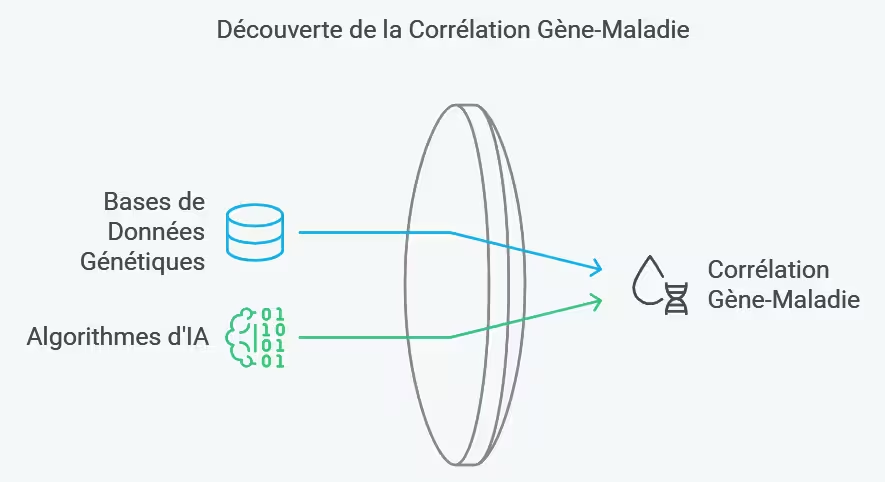
Infographie n°4 – Corrélation gènes-maladies : comment l’IA aide à identifier les variants pathogènes, image conservée de l’article original.
Confidentialité des données génomiques
Les données génomiques sont parmi les plus sensibles qui soient : elles sont uniques, permanentes, et révèlent des informations sur le patient (prédispositions aux maladies), mais aussi sur sa famille (consanguinité). Une fuite pourrait entraîner des discriminations à l’assurance, à l’embauche, ou dans l’accès aux prêts bancaires. Aux États-Unis, le GINA (Genetic Information Nondiscrimination Act) interdit certaines discriminations, mais la loi est imparfaite. En Europe, le RGPD s’applique, mais les bases de données génomiques restent des cibles de choix pour les cyberattaques. Le chiffrement, l’anonymisation robuste et la gouvernance des données sont des impératifs absolus.
Biais des algorithmes
Les modèles d’IA sont entraînés sur des données. Si les bases de données génomiques sont majoritairement composées d’individus d’origine européenne (ce qui a longtemps été le cas), les algorithmes seront moins performants pour les populations sous-représentées (personnes d’origine africaine, asiatique, amérindienne). Un variant génétique identifié comme « pathogène » chez les Européens pourrait être un variant bénin courant chez les Africains (et vice-versa). L’IA risque ainsi de creuser les inégalités de santé. Des efforts sont en cours pour diversifier les biobanques (All of Us aux États-Unis, H3Africa en Afrique).
Accessibilité et coût : une médecine à deux vitesses ?
Le séquençage génomique, bien qu’en baisse de coût, reste inabordable pour de nombreuses personnes dans les pays à revenu faible ou intermédiaire. De plus, l’interprétation par l’IA et le conseil génétique associé représentent des coûts supplémentaires. Si la médecine personnalisée se développe principalement dans les pays riches, le risque est l’apparition d’une médecine à deux vitesses : d’un côté, une médecine de précision high-tech pour les privilégiés ; de l’autre, une médecine « standard » pour les autres. Les décideurs politiques doivent intégrer ces nouvelles technologies dans des politiques de santé accessibles à tous, via le remboursement et la coopération internationale.
Recommandation éthique
Pour une médecine génomique juste et éthique, trois principes doivent guider les politiques publiques : 1) la transparence (les patients doivent comprendre comment leurs données sont utilisées), 2) l’équité (l’accès ne doit pas dépendre du revenu ou de l’origine), 3) la protection (les données doivent être sécurisées contre les usages discriminatoires). Des instances comme le Comité consultatif national d’éthique (CCNE) en France travaillent sur ces questions.
9. Perspectives 2026-2030 : médecine prédictive et thérapies géniques augmentées
L’avenir de la médecine génomique assistée par l’IA est prometteur. Voici les tendances qui se dessinent pour les années à venir.
Médecine prédictive à grande échelle
À mesure que le coût du séquençage diminue encore (objectif 100 € le génome d’ici 2030), on peut imaginer un dépistage génomique néonatal systématique, ou à l’âge adulte, pour identifier les prédispositions aux maladies (diabète, cancers, Alzheimer, maladies cardiovasculaires). L’IA analyserait les risques et proposerait des mesures préventives personnalisées (mode de vie, surveillance renforcée, voire traitements préventifs). Cette médecine prédictive soulève d’immenses questions éthiques (faut-il savoir qu’on a un risque élevé de maladie incurable ?), mais elle est techniquement à portée de main.
Thérapies géniques et édition du génome (CRISPR) assistées par IA
CRISPR-Cas9, la célèbre « ciseau moléculaire », permet de corriger des mutations génétiques in vivo. L’IA peut aider à concevoir les guides ARN (la « carte » qui dirige CRISPR) pour maximiser la précision et minimiser les coupures hors cible (effets secondaires). Des premières thérapies géniques ont déjà été approuvées (drépanocytose, amaurose congénitale). L’IA accélérera le développement de ces traitements pour des milliers de maladies génétiques rares.
Modèles multimodaux intégrant génome, environnement, mode de vie
La santé n’est pas uniquement génétique. L’environnement (pollution, alimentation), le mode de vie (exercice, sommeil) et le microbiote jouent un rôle majeur. Les futurs modèles d’IA seront multimodaux, intégrant les données génomiques avec les données des montres connectées, des capteurs environnementaux, des questionnaires alimentaires, etc. Cette approche holistique permettra une médecine véritablement personnalisée, tenant compte de l’ensemble des déterminants de la santé.
10. FAQ — Génome humain et IA
Un médecin peut-il déjà prescrire un séquençage complet du génome ?
Oui, dans certains pays (France, États-Unis, Royaume-Uni, Allemagne), un médecin (généraliste, généticien, oncologue) peut prescrire un séquençage complet du génome. En France, il est remboursé dans le cadre des filières « maladies rares » (diagnostic) et « cancer » (profil génomique des tumeurs) via le plan France Médecine Génomique 2030. Pour un patient « tout venant » sans pathologie identifiée, le séquençage n’est pas remboursé (il coûte environ 600 € en 2026).
Quelle est la différence entre le séquençage d’exome et le séquençage de génome complet ?
L’exome est la partie du génome qui code pour les protéines, soit environ 1 à 2 % de l’ADN total (20 000 gènes). Le séquençage d’exome (WES, Whole Exome Sequencing) est moins coûteux (environ 300 €) et plus rapide à analyser. Le séquençage de génome complet (WGS, Whole Genome Sequencing) séquence l’intégralité des 3 milliards de paires de bases, y compris les régions non codantes. Il est plus informatif (certaines maladies sont dues à des mutations dans des régions régulatrices) mais plus coûteux (600-800 €) et plus complexe à interpréter. En pratique clinique, on commence souvent par un WES, puis on passe au WGS si aucun diagnostic n’est trouvé.
Mon médecin peut-il prédire toutes les maladies que je vais avoir à partir de mon génome ?
Non, pas du tout. Pour quelques maladies « monogéniques » (liées à un seul gène), comme la maladie de Huntington ou la mucoviscidose, la présence de la mutation permet de prédire avec quasi-certitude le développement de la maladie. Mais pour les maladies « polygéniques » et complexes (diabète, hypertension, cancer, Alzheimer), le génome n’est qu’un facteur de risque parmi d’autres (environnement, mode de vie, hasard). L’IA peut calculer un « score de risque polygénique » (PRS) qui donne une probabilité statistique, mais pas une certitude. Avoir un risque élevé ne signifie pas qu’on développera la maladie, et inversement.
Mes données génomiques sont-elles protégées contre les fuites ?
En Europe, le RGPD impose des règles strictes : données anonymisées, consentement éclairé, droit d’accès et d’opposition, notification des fuites. Les hôpitaux et biobanques investissent dans la cybersécurité. Cependant, aucune protection n’est absolue. Des fuites ont déjà eu lieu (ex. fuite de données de 23andMe en 2023). La recommandation : pour les tests génétiques « grand public » (type 23andMe), soyez conscient des risques. Pour les tests médicaux en milieu hospitalier, la protection est généralement meilleure, mais la prudence reste de mise.
L’IA peut-elle déjà diagnostiquer des maladies à partir du génome ?
Oui, pour les maladies génétiques rares, l’IA est un outil d’aide au diagnostic de plus en plus performant. Des plateformes comme Emedgene, Franklin ou VarSome analysent les variants génétiques, les comparent aux bases de données et à la littérature, et proposent un diagnostic probable. Dans des études, ces systèmes atteignent une précision comparable à celle d’un expert humain, mais plus rapidement. Cependant, le diagnostic final est toujours validé par un médecin généticien. Pour les maladies complexes (cancer, diabète), l’IA est utilisée pour prédire des risques ou guider les traitements, mais pas pour « diagnostiquer » au sens classique.
La médecine personnalisée est-elle accessible à tous en France ?
En France, l’accès à la médecine génomique se développe, mais il reste inégal. Les filières « maladies rares » et « cancer » sont prises en charge par l’Assurance maladie via le plan France Génomique 2030. Les patients qui n’entrent pas dans ces filières (ex. personne souhaitant un dépistage préventif) doivent payer de leur poche (environ 600 € pour un génome complet). Il existe également des inégalités territoriales : les centres de génétique sont concentrés dans les grandes villes. La généralisation du séquençage en routine clinique est un objectif pour 2030, mais le chemin est encore long.
Articles connexes
Pour approfondir les thèmes de l’IA dans la santé et de la médecine personnalisée, voici d’autres contenus disponibles sur iana-data.org.
Comment l’IA transforme le diagnostic dans toutes les spécialités médicales.
Les enjeux de la protection des données de santé.
Une introduction aux concepts de médecine de précision.
Sources
- Human Genome Project – Archives et publications (2001-2003, NIH)
- National Human Genome Research Institute (NHGRI) – The cost of sequencing a human genome (mise à jour 2026)
- DeepMind – AlphaFold protein structure database (2021-2025)
- UK Biobank – Genomic data release (2025 update)
- France Génomique – Rapport d’activité 2025 (ministère de l’Enseignement supérieur et de la Recherche)
- Foundation Medicine – Clinical validation of AI-based genomic profiling (2025)
- Rare Genomics Institute – AI for rare disease diagnosis (2024)
- Comité consultatif national d’éthique (CCNE) – Avis sur la médecine génomique (2025)
- Loi de bioéthique française (2021, révision 2025)
- All of Us Research Program (NIH) – Data release 2026





