Dans les chambres d’hôpital, des capteurs analysent en continu le rythme cardiaque, la respiration et les mouvements d’un patient âgé, sans qu’il ait besoin de porter le moindre fil. Au domicile d’un insuffisant cardiaque, une montre connectée transmet chaque jour ses paramètres vitaux à son cardiologue, qui peut ajuster son traitement à distance. Dans les services de réanimation, des algorithmes d’IA préviennent les équipes soignantes plusieurs heures avant qu’une dégradation brutale ne survienne. L’intelligence artificielle est en train de révolutionner la surveillance des patients — une révolution silencieuse, discrète, mais aux conséquences immenses sur la qualité des soins, la sécurité des patients et l’organisation des systèmes de santé. Cet article explore ces avancées, leurs bénéfices concrets, et les défis qu’il reste à relever.
L’IA pour la surveillance des patients désigne l’ensemble des technologies algorithmiques et des dispositifs connectés qui permettent de collecter, d’analyser et d’interpréter en temps réel des données médicales (paramètres vitaux, mouvements, comportements) afin de détecter précocement des anomalies, des signes de détérioration, ou des risques de complication. L’objectif ultime est de permettre une intervention plus rapide et plus ciblée des professionnels de santé, améliorant ainsi la sécurité et la qualité des soins tout en réduisant la charge de travail du personnel soignant.
Ces technologies se déclinent sous différentes formes : des capteurs environnementaux placés dans les chambres d’hôpital (sous le matelas, au plafond) qui mesurent la fréquence cardiaque, la respiration et les mouvements sans contact ; des dispositifs portables connectés (montres, bracelets, patchs) que le patient porte sur lui ; des systèmes d’analyse prédictive qui croisent les données du dossier médical électronique avec les flux en temps réel pour alerter sur un risque de septicémie, d’arrêt cardiaque ou de chute. Dans tous les cas, l’IA joue le rôle d’un « vigile silencieux » : elle surveille en continu, ne se fatigue pas, ne cligne pas des yeux, et ne signale que ce qui est vraiment anormal — évitant ainsi la « fatigue d’alarme » qui guette les soignants.
L’IA de surveillance ne remplace pas le jugement clinique. Elle alerte, suggère, prédit — mais c’est toujours un médecin ou un infirmier qui prend la décision finale. L’IA est un outil d’aide à la décision, pas un automate de soin. Cette distinction est cruciale pour comprendre son rôle et ses limites.
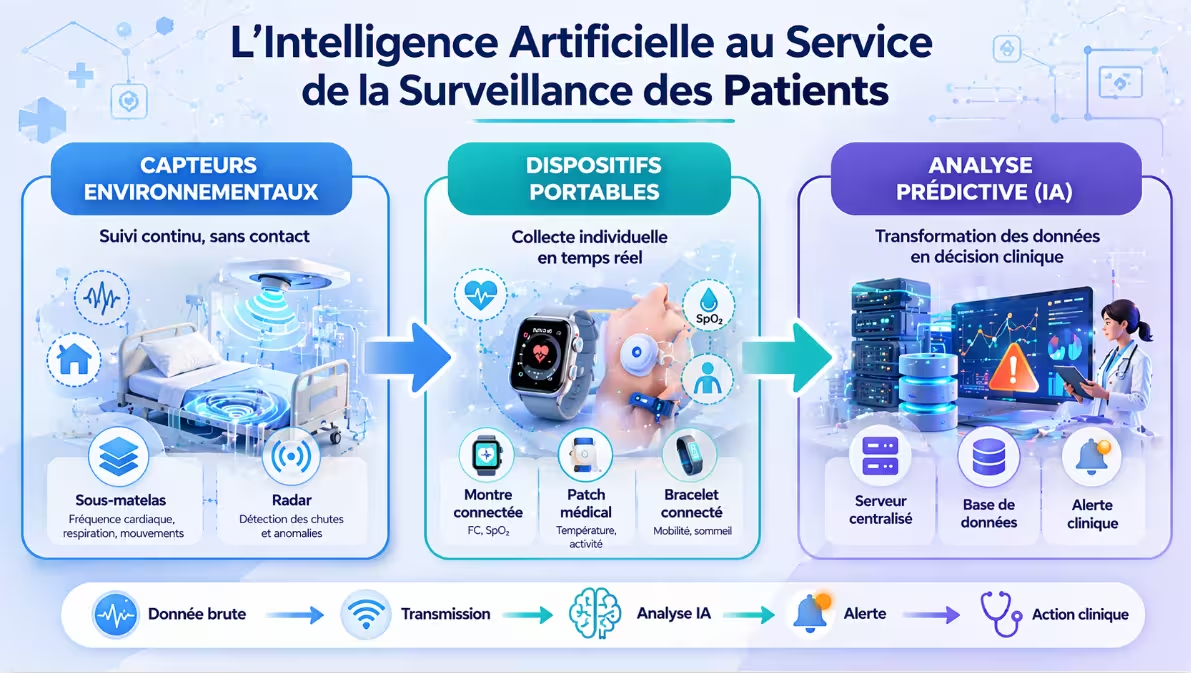
Infographie n°1 – Panorama des technologies de surveillance par IA : capteurs environnementaux, dispositifs portables, analyse prédictive.
L’idée de surveiller les patients à distance n’est pas nouvelle, mais c’est l’arrivée de l’IA qui a véritablement révolutionné ce domaine en le faisant passer d’une surveillance « réactive » à une surveillance « proactive ».
Les débuts (années 1960-1980) : Les premiers moniteurs cardiaques font leur apparition dans les unités de soins intensifs. Ils affichent en temps réel le rythme cardiaque et la pression artérielle, mais tout repose sur l’œil humain : un infirmier doit regarder régulièrement les écrans et interpréter les courbes. Les faux positifs (alarmes pour des variations normales) sont nombreux, entraînant une « fatigue d’alarme » bien documentée.
L’arrivée des premiers algorithmes (années 1990-2000) : Des systèmes experts simples (basés sur des règles « si… alors… ») sont intégrés aux moniteurs. Ils déclenchent une alarme si la fréquence cardiaque dépasse un seuil prédéfini. Mais ces systèmes ne « comprennent » pas le contexte : une tachycardie bénigne due à la douleur ou à l’anxiété déclenche la même alarme qu’une tachycardie annonçant un arrêt cardiaque.
La révolution des données massives et du machine learning (années 2010-2020) : La généralisation des dossiers médicaux électroniques, la baisse du coût des capteurs, et l’essor des dispositifs portables (Fitbit, Apple Watch) créent un déluge de données. Les algorithmes de machine learning (forêts aléatoires, réseaux de neurones) apprennent à reconnaître des motifs prédictifs invisibles à l’œil humain. Des systèmes comme EarlySense (capteur sous-matelas) ou Philips eCareCoordinator montrent qu’ils peuvent prédire une dégradation jusqu’à 6 à 8 heures avant qu’elle ne soit cliniquement visible.
La maturité (2020-2026) : L’IA est désormais intégrée dans les flux de travail hospitaliers. Les alertes sont plus précises (moins de faux positifs), contextualisées (l’IA sait que le patient vient de faire de l’exercice ou de recevoir un médicament), et priorisées (alerte « critique » vs « information »). La pandémie de COVID-19 a agi comme un accélérateur : la télésurveillance des patients à domicile est devenue une nécessité, et l’IA a prouvé sa valeur.
Le développement rapide de l’IA dans la surveillance des patients répond à plusieurs besoins structurels des systèmes de santé contemporains.
Dans tous les pays développés, la proportion de personnes âgées de plus de 65 ans ne cesse d’augmenter. Les personnes âgées sont plus susceptibles de souffrir de maladies chroniques (insuffisance cardiaque, BPCO, diabète, hypertension) qui nécessitent une surveillance régulière. Les hôpitaux n’ont pas la capacité de garder ces patients en hospitalisation prolongée ; la surveillance à domicile (télésurveillance) devient une nécessité. L’IA permet de surveiller des centaines, voire des milliers de patients à domicile avec une équipe médicale réduite.
Les services hospitaliers sont sous tension. Les infirmiers et aides-soignants sont débordés, le turnover est élevé, et le burnout est devenu un problème majeur de santé publique. L’IA ne remplace pas les soignants, mais elle les soulage d’une partie de la charge mentale : elle surveille en continu, alerte uniquement en cas de réel problème, et automatise la collecte de données (évitant aux infirmiers de devoir noter manuellement les constantes toutes les heures). Des études montrent que l’IA peut réduire de 30 à 40 % le temps passé par les infirmiers à la surveillance de routine.
Trois avancées techniques ont rendu la surveillance IA possible à grande échelle. D’abord, la miniaturisation des capteurs : on peut désormais mesurer la fréquence cardiaque, la saturation en oxygène, la température, l’activité, et même l’ECG à 3 dérivations via un patch adhésif de la taille d’une pièce de 2 euros. Ensuite, la 5G permet de transmettre en temps réel des flux de données volumineux (vidéo, capteurs multiples) depuis le domicile du patient. Enfin, l’edge computing (traitement local sur le dispositif, sans envoyer toutes les données au cloud) préserve la confidentialité et réduit la latence.
Les systèmes de santé sont payés à l’acte ou à la performance. Réduire la durée moyenne de séjour et le taux de réadmission à 30 jours est un objectif majeur. La télésurveillance post-opératoire ou pour les maladies chroniques permet de sortir le patient plus tôt de l’hôpital tout en assurant sa sécurité, réduisant ainsi les coûts. Des études montrent que chaque euro investi dans la télésurveillance IA génère 3 à 5 euros d’économies (moins d’hospitalisations, moins de passages aux urgences).
Selon une étude de l’AP-HP (2025), le déploiement d’un système de télésurveillance IA pour l’insuffisance cardiaque a permis de réduire les réadmissions à 30 jours de 38 % et de générer une économie nette de 4 200 € par patient et par an, principalement grâce à la diminution des hospitalisations évitées.
Voici un tableau récapitulatif des principales applications de l’IA dans la surveillance des patients, avec des exemples concrets et des niveaux de maturité.
| Application | Description | Exemples / Références | Niveau de maturité |
|---|---|---|---|
| Capteurs environnementaux sans contact | Capteurs sous le matelas ou au plafond mesurant la fréquence cardiaque, la respiration, les mouvements, sans que le patient porte rien. Détection des chutes, des arrêts respiratoires, des dégradations. | EarlySense, Oxitone, Neteera (capteur radar) | Déployé dans plusieurs centaines d’hôpitaux (USA, Europe, Israël). Remboursé par certaines assurances. |
| Dispositifs portables grand public | Montres, bagues, bracelets qui mesurent l’activité, le sommeil, la fréquence cardiaque, l’ECG, la saturation. Alertes en cas d’arythmie, de chute. | Apple Watch (arythmie, ECG), Fitbit, Oura Ring, Withings | Très mature pour la prévention et le bien-être. Utilisation clinique émergente (prescription par certains médecins). |
| Patchs et dispositifs médicaux connectés | Patchs adhésifs portés plusieurs jours, mesurant ECG, température, activité. Utilisés pour le monitoring post-opératoire ou pour les maladies chroniques. | Philips BioSticker, Zio Patch (ECG), Dexcom G7 (glucose, diabète) | Mature, remboursé dans certains pays pour des indications précises (diabète, détection d’arythmies). |
| Analyse prédictive des risques | Algorithmes analysant les données du dossier médical électronique + flux temps réel pour prédire septicémie, arrêt cardiaque, détérioration respiratoire, risque de chute. | Epic Sepsis Model, Philips eCareCoordinator, Cerner HealtheIntent | En déploiement dans les grands hôpitaux. Validité clinique prouvée pour certaines prédictions (septicémie). |
| Télésurveillance à domicile | Plateformes intégrant capteurs portables + questionnaires + IA, permettant aux patients chroniques ou post-opératoires d’être suivis à domicile. Alertes envoyées à l’équipe soignante. | Current Health (Best Buy), Biofourmis, ResMed, Air Liquide Healthcare | Fort développement depuis COVID. Remboursé dans plusieurs pays (France : ETAPES, puis Forfait Télésurveillance). |
Tableau des principales applications de l’IA en surveillance des patients, mis à jour en 2026.
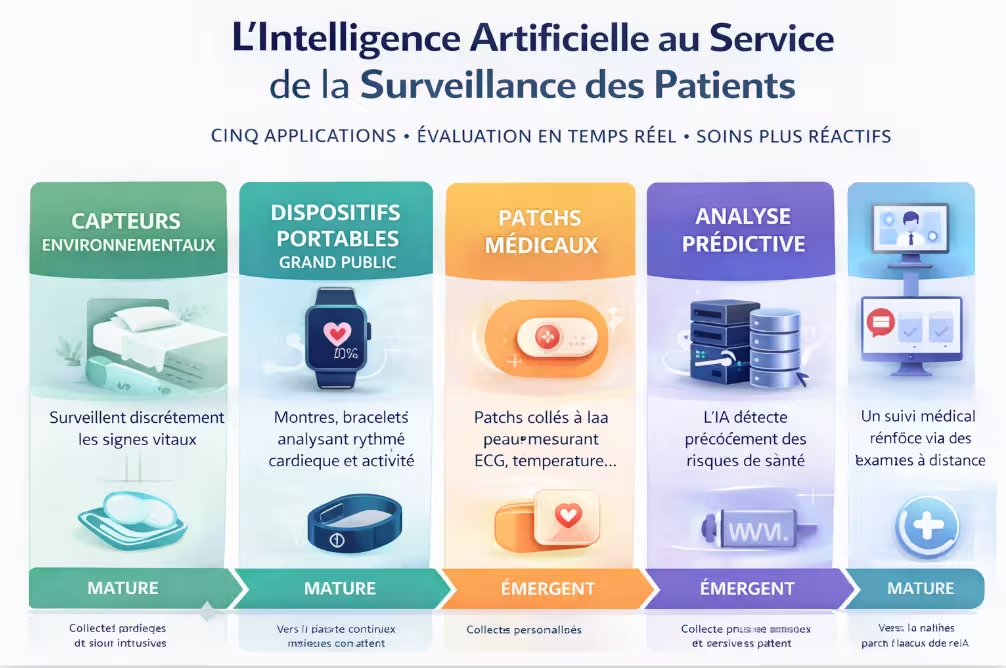
Infographie n°2 – Les cinq grandes familles d’applications : capteurs environnementaux, dispositifs portables, patchs médicaux, analyse prédictive, télésurveillance à domicile.
L’IA dans la surveillance des patients a des conséquences tangibles, positives pour la plupart, mesurables en termes cliniques et économiques.
Des études cliniques montrent que l’IA prédictive réduit significativement les événements indésirables. Par exemple, le système EarlySense a démontré une réduction de 50 % des arrêts cardiorespiratoires dans les unités de soins généraux (non spécialisés) et une réduction de 45 % des transferts en soins intensifs. En détectant les signes de dégradation plusieurs heures à l’avance, l’équipe soignante peut intervenir préventivement (changer un traitement, augmenter l’oxygénothérapie, transférer le patient) avant que la situation ne devienne critique.
La télésurveillance à domicile permet aux patients de sortir plus tôt de l’hôpital et d’éviter des réadmissions évitables. Pour l’insuffisance cardiaque, pathologie responsable de nombreuses hospitalisations, les programmes de télésurveillance IA réduisent les réadmissions à 30 jours de 30 à 40 %. Le patient est plus rassuré, l’hôpital libère des lits, et les coûts baissent.
Les dispositifs connectés rappellent au patient de prendre ses médicaments, d’effectuer ses exercices de rééducation, ou de répondre à des questionnaires d’évaluation. L’IA adapte les rappels en fonction du comportement du patient. Cette personnalisation améliore l’observance thérapeutique, un facteur clé de succès pour les maladies chroniques.
Les infirmiers passent un temps considérable à mesurer manuellement les constantes vitales (pouls, tension, température, saturation) et à les noter dans le dossier. L’IA automatise cette collecte : les capteurs transmettent directement les données au dossier médical électronique. Les soignants peuvent consacrer ce temps à des tâches à plus forte valeur ajoutée : soins relationnels, éducation du patient, accompagnement. Dans une étude de l’AP-HP, le temps infirmier consacré à la surveillance de routine a diminué de 35 % après le déploiement de capteurs connectés.
L’Assistance Publique – Hôpitaux de Paris a déployé un programme de télésurveillance IA pour les patients insuffisants cardiaques. Les patients reçoivent un kit comprenant une balance connectée, un tensiomètre, et une application mobile. Les données sont analysées par un algorithme qui détecte les signes de décompensation (prise de poids brutale, chute de tension). En cas d’alerte, une infirmière appelle le patient et ajuste le traitement ou organise une consultation rapide. Bilan après deux ans : réduction de 38 % des réadmissions, satisfaction patient élevée (89 %), et économies significatives.
Le système de surveillance IA du Mount Sinai analyse en continu les données des moniteurs de 150 lits de réanimation. L’algorithme prédit le risque de septicémie jusqu’à 12 heures avant l’apparition des symptômes cliniques. Le taux de mortalité par septicémie a diminué de 25 % depuis le déploiement.
Le capteur EarlySense se place sous le matelas, sans contact, et mesure la fréquence cardiaque, la respiration et les mouvements. Il est utilisé dans des centaines d’hôpitaux aux États-Unis, en Europe et en Israël, principalement dans les unités de soins généraux (non intensifs) où les patients ne sont pas surveillés en continu. Le système a démontré une réduction de 86 % des événements de code bleu (arrêt cardiaque) dans une étude clinique.
Current Health (racheté par Best Buy) fournit un bracelet connecté qui mesure la saturation, la fréquence cardiaque, la température, et les pas. Pendant la pandémie, des milliers de patients COVID-19 ont été surveillés à domicile, avec des alertes envoyées aux médecins en cas de chute de saturation (signe de pneumonie sévère). Le système a permis de désengorger les hôpitaux et d’éviter des admissions inutiles.
Malgré ses promesses, l’IA dans la surveillance des patients n’est pas sans risques ni défis. Une approche équilibrée est nécessaire.
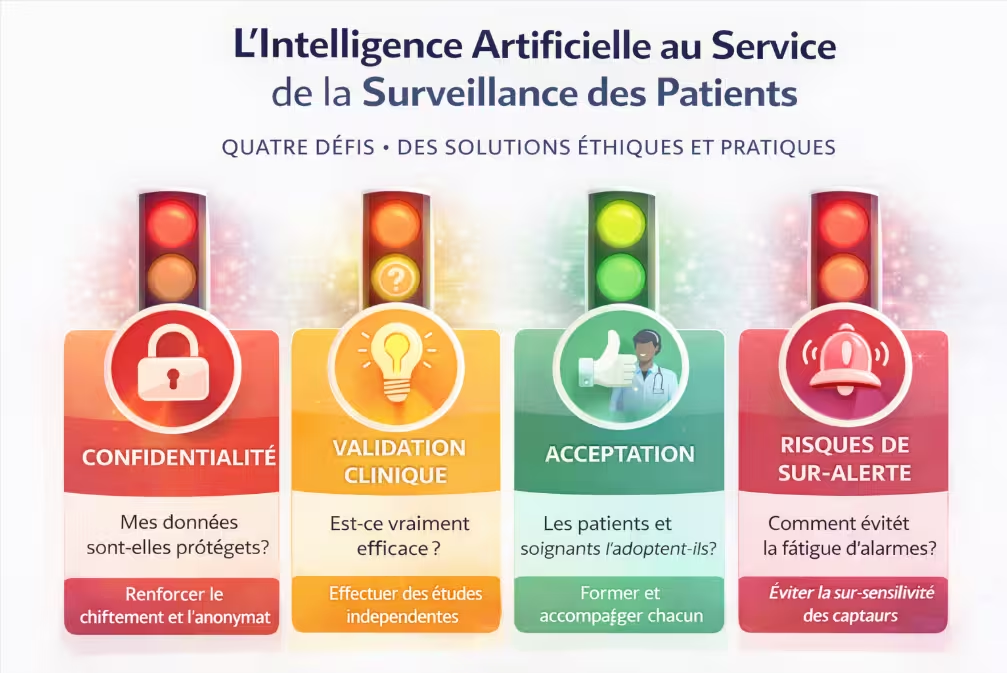
Infographie n°3 – Les quatre grands défis : confidentialité des données, validation clinique, acceptation par les soignants, risques de sur-alerte.
Les systèmes de surveillance collectent des données de santé extrêmement sensibles : fréquence cardiaque, respiration, mouvements, parfois vidéo. Ces données, si elles sont mal protégées, peuvent être piratées ou utilisées à des fins discriminatoires (assurances, employeurs). Les hôpitaux et fournisseurs doivent respecter des normes strictes (RGPD en Europe, HIPAA aux États-Unis), chiffrer les données, et obtenir le consentement éclairé des patients. La surveillance « invisible » (capteurs sans contact) soulève des questions spécifiques : le patient sait-il qu’il est surveillé ? A-t-il donné son consentement explicite ? Les hôpitaux doivent afficher clairement la présence de ces dispositifs et expliquer leur fonctionnement.
Les algorithmes d’IA ne sont pas parfaits. Un faux positif (alarme alors qu’il n’y a pas de problème réel) génère une fatigue d’alarme et peut conduire les soignants à ignorer les alertes suivantes. Un faux négatif (absence d’alarme alors qu’il y a un problème réel) est encore plus grave : le patient peut se dégrader sans que personne n’intervienne. La validation clinique des systèmes d’IA doit être rigoureuse, sur des populations diverses, avant leur déploiement en routine. Les autorités de santé (FDA aux États-Unis, HAS en France, CE marquage) jouent un rôle de garde-fou.
Certains patients peuvent se sentir « espionnés » ou déshumanisés par une surveillance automatisée, surtout s’ils ne comprennent pas comment fonctionne le système. D’autres, au contraire, se sentent rassurés. L’information et la pédagogie sont essentielles. Du côté des soignants, la méfiance est fréquente : « l’IA va-t-elle remplacer mon jugement ? », « cet algorithme est-il fiable ? », « vais-je recevoir des alertes sans arrêt ? ». La formation et l’implication des soignants dans le choix et le paramétrage des systèmes sont des facteurs clés d’acceptation.
Pour un déploiement réussi et éthique de l’IA de surveillance : 1) Impliquez les soignants dès la phase de choix du système, 2) Formez-les à l’interprétation des alertes (ne pas les suivre aveuglément), 3) Informez les patients et obtenez leur consentement explicite, 4) Mettez en place une gouvernance des données claire, 5) Évaluez régulièrement les performances du système (taux de faux positifs, délai d’intervention, satisfaction).
Le domaine évolue rapidement. Plusieurs tendances se dessinent pour les années à venir.
Les capteurs deviennent invisibles : patchs de la taille d’un timbre, vêtements connectés (t-shirts qui mesurent l’ECG), capteurs radar qui traversent les vêtements, caméras thermiques qui mesurent la température sans contact. La multimodalité (combiner plusieurs types de capteurs) améliore la précision : un algorithme peut croiser les données du capteur sous-matelas (respiration, rythme cardiaque) avec celles d’une caméra (détection de chute) et d’un micro (bruits de détresse).
Les alertes de l’IA ne sont plus isolées : elles s’intègrent directement dans le flux de travail du DME (par exemple, Epic, Cerner, Orbis, Easily). L’infirmier voit une alerte priorisée dans son tableau de bord, avec un lien direct vers les données du patient. L’IA peut également suggérer des actions (ex. « administrer oxygène », « prévenir le médecin », « transférer en soins intensifs »). Cette intégration réduit la friction et accélère la prise de décision.
La télésurveillance IA s’étend au-delà de l’insuffisance cardiaque et du diabète : cancer (surveillance des effets secondaires des chimiothérapies), BPCO, maladie rénale chronique, santé mentale (détection des signes de rechute dépressive via l’analyse de la voix et de l’activité). Les forfaits de télésurveillance se généralisent, avec un remboursement dans de plus en plus de pays.
Les nouveaux systèmes ne se contentent pas d’alerter : ils génèrent des résumés en langage naturel des évolutions du patient. « Au cours des dernières 24 heures, le patient a présenté une légère tachycardie entre 2h et 4h, sans autre anomalie. Il s’est levé 3 fois, dont une fois à 3h15. » Le médecin gagne un temps précieux à la lecture du compte rendu. Cette fonction, rendue possible par les LLM (GPT-4o, Gemini), commence à être intégrée dans les plateformes haut de gamme.
Non, absolument pas. L’IA ne remplace pas le jugement clinique, le contact humain, les soins relationnels, ni la capacité à prendre des décisions complexes. Elle soulage les infirmiers des tâches répétitives (prise de constantes, surveillance de routine) et les alerte en cas de problème, leur permettant de se concentrer sur les soins à haute valeur ajoutée. Des études montrent que l’IA améliore la satisfaction au travail des infirmiers (moins de stress, moins de charge mentale) et réduit le burnout, sans supprimer d’emplois.
Oui, depuis 2022 (expérimentation ETAPES) et plus largement depuis 2024 avec le forfait de télésurveillance (article 51). Plusieurs pathologies sont éligibles : insuffisance cardiaque, insuffisance rénale chronique, diabète, BPCO, traitement par ventilation à domicile, post-cancer. Le forfait comprend la fourniture des dispositifs (balance, tensiomètre, oxymètre) et le suivi par une équipe médicale. Le patient n’avance pas les frais. Le déploiement est progressif, mais la tendance est à la généralisation.
Les risques existent, comme pour tout objet connecté. Un pirate pourrait : modifier les données (faisant croire à une détérioration ou au contraire masquer un vrai problème), déclencher de fausses alarmes, ou voler les données de santé pour les revendre. Les fabricants sérieux intègrent des protections : chiffrement des données, authentification forte, mises à jour de sécurité régulières, isolation des dispositifs sur des réseaux dédiés. Les hôpitaux doivent auditer régulièrement leur cybersécurité. En cas d’utilisation à domicile, les risques sont moindres mais existent ; il est conseillé d’utiliser des dispositifs certifiés (marquage CE médical, FDA) et de suivre les recommandations de sécurité (mot de passe fort, mise à jour du smartphone).
Oui, c’est un domaine de recherche actif. Des capteurs environnementaux (détecteurs de mouvement, capteurs de porte, caméras thermiques) peuvent détecter des comportements à risque : errance nocturne, oubli de fermeture du gaz, chute. L’IA peut alerter l’aidant familial ou un centre d’appel. Des études montrent que ces systèmes réduisent l’anxiété des aidants et permettent de maintenir les patients à domicile plus longtemps. Cependant, des questions éthiques se posent (consentement du patient s’il n’est plus en capacité de le donner, respect de l’intimité). Des garde-fous sont nécessaires.
La précision est bonne, mais pas parfaite. Pour la détection de la fibrillation auriculaire (FA), l’Apple Watch a une sensibilité d’environ 90 % (elle détecte 90 % des vrais cas) et une spécificité d’environ 98 % (elle ne se trompe que 2 % du temps). C’est suffisant pour un outil de dépistage de premier niveau, mais un diagnostic formel nécessite un ECG de référence. L’alerte « rythme irrégulier » doit conduire à consulter un médecin, pas à s’auto-médiquer. La FDA et les autorités européennes ont validé ces dispositifs pour le dépistage, pas pour le diagnostic.
Cela dépend des patients et de l’information qui leur est donnée. Dans les études, la majorité des patients acceptent la surveillance par IA lorsqu’elle est expliquée et qu’elle apporte un bénéfice clair (sécurité, réduction des hospitalisations). Les patients âgés sont parfois plus méfiants, mais une explication adaptée lève la plupart des craintes. Les patients jeunes et familiers de la technologie sont très demandeurs. La clé est la transparence : expliquer quelles données sont collectées, par qui, combien de temps, et à quelles fins. Le consentement explicite est obligatoire dans la plupart des pays.